En France, le rituximab est commercialisé sous le nom de marque MabThéra par les laboratoires Roche, dans certains lymphomes et leucémies et dans la polyarthrite rhumatoïde. Il fait partie des anticorps monoclonaux, que j’évoque souvent sur Pharmacritique, de même que Tysabri, Avastin, Humira, Enbrel, Herceptin, Raptiva (retiré du marché aussi à cause de leucoencéphalopathies LEMP), Remicade, Cimzia, Xolair…
Je détaille la dernière alerte de Santé Canada, en juin 2011, pour plusieurs cas de décès liés à la perfusion de MabThéra, puis les alertes précédentes des autorités sanitaires canadiennes et françaises sur les leucoencéphalopathies multifocales progressives (LEMP). Sans oublier les mises en garde portant sur d’autres effets indésirables, tous avec quelques cas mortels, tels qu’une réactivation d’une hépatite B, des occlusions et perforations intestinales, des réactions cutanées sévères…
Une alerte de 2009 de la FDA nous apprend qu’un décès par LEMP peut survenir jusqu’à un an et demi après l’arrêt du traitement par MabThéra.

Je rappelle aussi d’autres effets indésirables communs à toute la classe des anticorps monoclonaux, en donnant des liens, y compris vers le verdict très sévère des revues indépendantes Arznei-Telegramm, Prescrire et Butlleti Groc. J’aborde l’infection opportuniste par le virus JC à l’origine de la LEMP et finis par reposer la question d’une évaluation globale de ces biomédicaments, d’autant plus nécessaire que le progrès thérapeutique qui leur est reconnu est faible, voire très faible, pour la plupart d’entre eux, pour des coûts astronomiques habituels dès qu’il s’agit de biotechnologie.
Le rapport benefices/risques n’est pas le même dans un cancer ou dans les maladies auto-immunes. Ce problème se pose de plus en plus, compte tenu du marketing agressif et des demandes d’extensions d’indication.
Description du rituximab et indications en France (selon Oncoprof, la HAS et l’AFSSAPS)
« Le rituximab (Mabthéra™ ou Rituxan™ [ou Rixathon]) est un anticorps chimérique murin humanisé contre l’antigène CD 20, comportant d’une part les régions constantes d’une IgG1 humaine et d’autre part les régions variables des chaînes légères et lourdes d’origine murine. C’est un pur produit du génie génétique.
Il est actif contre les cellules malignes présentant l’antigène CD 20, (…) c’est-à-dire dans les lymphomes folliculaires de stade III-IV et dans les lymphomes non-hodgkinien agressifs diffus à grandes cellules B, CD20 positif. »
La Commission de transparence de la Haute Autorité de Santé (HAS) lui reconnaît, dans un avis de juillet 2009, un « progrès thérapeutique majeur de l’association MABTHERA + chimiothérapie par rapport à la chimiothérapie seule dans le traitement de première ligne du lymphome folliculaire de stade III-IV ».
Selon l’AFSSAPS (agence française du médicament), « MabThera® est également indiqué en association au méthotrexate, pour le traitement de la polyarthrite rhumatoïde (PR) active, sévère, chez les patients adultes qui ont présenté une réponse inadéquate ou une intolérance aux traitements de fond, dont au moins un anti-TNF (inhibiteur du facteur de nécrose tumorale). MabThera® n’est pas indiqué dans d’autres maladies auto-immunes. »
Indications du MabThéra, identiques en France et au Canada
« RITUXAN [MabThéra, Rixathon] est indiqué pour le traitement du lymphome non hodgkinien (LNH) de type B et de la leucémie lymphoïde chronique de type B jamais traitée (LLC B) au stade B ou C; il est aussi indiqué, en association avec le méthotrexate, pour soulager les signes et les symptômes de la polyarthrite rhumatoïde évolutive modérée ou grave chez les adultes ayant montré une réponse inadéquate ou une intolérance à un ou plusieurs traitements par des inhibiteurs du facteur de nécrose tumorale (anti-TNF). »
En septembre 2009, l’agence états-unienne du médicament FDA rendait public un cas de décès par leucoencéphalopathie multifocale progressive un an et demi après l’arrêt du traitement d’une arthrite rhumatoïde par MabThéra (rituximab, Rituxan aux Etats-Unis. Rixathon est un biosimilaire plus récent).
MabThéra / Rituxan / Rixathon est le deuxième médicament le plus vendu de Genentech – firme de biotechnologie qui commercialisait bon nombre d’anticorps monoclonaux avant d’être rachetée par Roche -, avec un chiffre de ventes de 2,3 milliards de dollars en 2007, juste derrière Avastin.
Genentech a souligné que la relation de cause à effet entre la LEMP de cette femme et le MabThéra n’était pas certaine, parce qu’elle prenait plusieurs traitements. Sauf que l’on sait parfaitement que toute la classe d’anticorps monoclonaux compte la leucoencéphalopathie multifocale progressive parmi ses effets indésirables de classe, et que la LEMP n’apparaît que chez des personnes ayant un traitement immunosuppresseur, ou alors immunodéprimé à cause d’affections telles que le SIDA.
Echec du MabThéra/ Rituxan dans le lupus
Mais il n’est pas étonnant que Genentech essaie de sauver les meubles. En avril 2008, la même année où ce décès a été signalé, un essai clinique de phase II et III, randomisé contrôlé en double aveugle, étalé sur 52 semaines, n’a pas montré d’efficacité du MabThéra (rituximab) par rapport au placebo chez des patients atteints de lupus systémique érythémateux sévère. L’échec ne se limite pas au critère principal de jugement ; il est total, car les résultats ont été négatifs aussi selon les six critères secondaires de jugement. Or Genentech espérait un surplus d’un milliard de dollars de chiffres de vente en cas d’autorisation de mise sur le marché, ou plutôt d’extension d’indication, dans l’indication « lupus ».
Hal Barron, l’un des responsables de la recherche et développement, a exprimé sa déception face aux résultats. Mais Genentech ne baisse pas les bras, car un autre essai clinique est en cours chez des patients atteints de néphrite de lupus (inflammation des reins, dans le cadre du lupus systémique érythémateux).
Parlant de lupus, des cas de leucoencéphalite multifocale progressive ont été signalés aussi chez des patients traités par MabThéra/ Rituxan hors AMM, et notamment pour un lupus… Bref, voilà un médicament qui montre son inefficacité et même tue dans l’indication lupus, ce qui n’empêche pas les laboratoires Genentech et Biogen Idec – qui le commercialisent ensemble aux Etats-Unis -, de tenter le coup… Et Roche continue sur cette lancée.
Car Ed Silverman nous apprend sur le blog Pharmalot que Genentech/Roche est en train de tester une classe d’autres biomédicaments qui seraient une variante plus atténuée d’anticorps monoclonaux : des anticorps anti CD 20, agissant selon le même mécanisme, classe pour laquelle la firme espère obtenir des autorisations de mise sur le marché dans toutes les maladies auto-immunes et qui est testée dans des essais cliniques de phase III pour l’arthrite rhumatoïde et de phase II pour la sclérose en plaques. Il semblerait que les analystes financiers soient sceptiques quant aux chances de succès, vu que les anticorps les plus puissants tels que MabThéra/Rituxan n’aient montré aucune efficacité. D’ailleurs, le cours en bourse de l’action Genentech et Biogen Idec est descendu en flèche après l’annonce de l’échec de l’essai clinique du Rituxan chez les patients lupiques.
Santé Canada signale des réactions sévères et mortelles sous MabThéra, liées à la perfusion
Au Canada, le rituximab est commercialisé sous le même nom de marque qu’aux Etats-Unis : Rituxan, par Hoffmann Laroche.
Voici l’extrait essentiel de l’annonce du 7 juin 2011, à travers une lettre de la firme Hoffmann Laroche
« Des réactions graves et mortelles liées à la perfusion ont été signalées chez quatre personnes atteintes de polyarthrite rhumatoïde auxquelles RITUXAN avait été administré. Aucun de ces cas ne provenait du Canada.
Une réaction liée à la perfusion peut se manifester comme suit : fièvre, frissons, difficulté à respirer, serrement dans la poitrine et/ou à la gorge, maux d’estomac, éruption cutanée. Avisez votre professionnel de la santé si vous présentez l’un de ces symptômes.
En cas de réaction grave liée à la perfusion de RITUXAN, l’administration du médicament doit être interrompue. Étant donné que des réactions graves peuvent se produire pendant la perfusion de RITUXAN, il est important qu’un professionnel de la santé vous surveille de près pendant et après la perfusion, surtout si vous avez des problèmes cardiaques. Avant la perfusion de RITUXAN, il est important que vous receviez un médicament qui fait baisser la fièvre (comme TYLENOL® [paracétamol], un antihistaminique (comme BENADRYL® [Nautamine en France], et un stéroïde (comme la prednisone). »
Leucoencéphalopathies multifocales progressives selon les autorités sanitaires canadiennes

Voici une alerte du 21 octobre 2009 (lettre de Hoffmann Laroche, reprise sur le site de Santé Canada), sur la LEMP (voir définition plus bas) :
« Suite à l’examen des rapports récents d’innocuité post-commercialisation :
Un troisième cas de leucoencéphalopathie multifocale progressive (LMP) a été signalé chez un patient atteint d’arthrite rhumatoïde traité avec RITUXAN. Il s’agit du premier cas de LMP chez un patient atteint de polyarthrite rhumatoïde recevant RITUXAN et n’ayant jamais été traité avec d’autres agents immuno-modulateurs biologiques puissants. »
(Image de Medscape)
Le point d’information donne des détails sur deux autres cas mortels de leucoencéphalopathie multifocale progressive au Canada :
« Dans le passé, 2 cas mortels de LMP [LEMP] confirmée avaient été signalés chez des patients atteints de polyarthrite rhumatoïde traités avec RITUXAN [nom canadien du MabThéra]. Ces cas concernaient une femme de 51 ans et une autre de 73 ans présentant des facteurs de risque potentiels de LMP, dont un cancer oropharyngien traité avec chimiothérapie et radiothérapie et/ou une lymphopénie de longue date avant et pendant le traitement avec RITUXAN.
Le cas le plus récent concerne une femme de 73 ans ayant reçu un diagnostic de polyarthrite rhumatoïde [PR] séronégative il y a 3 ans. (…) Elle a reçu un cycle de traitement avec RITUXAN (1000 mg administrés à 2 semaines d’intervalle). La patiente a présenté des dysesthésies et une ataxie 4 à 6 mois après le traitement avec RITUXAN. La LMP a été diagnostiquée en fonction des symptômes cliniques, des observations par IRM et de la détection d’ADN du virus JC dans le LCR par technique PCR.
L’incidence globale des cas de LMP chez les patients atteints de PR traités avec RITUXAN est faible (3 cas sur environ 100 000 patients). Le mécanisme potentiel derrière l’apparition de la LMP en relation avec RITUXAN demeure inconnu, mais un rôle contributif ne peut être écarté. Selon les données recueillies jusqu’à présent, les médecins devraient considérer que RITUXAN peut augmenter le risque de LMP chez les patients atteints de PR.
Les médecins doivent envisager un diagnostic de LMP chez tout patient traité avec RITUXAN qui présente de nouvelles manifestations neurologiques. Une consultation avec un neurologue, un examen du cerveau par IRM et une ponction lombaire (pour le dépistage du virus JC par technique PCR) sont des interventions cliniques recommandées. En cas d’apparition d’une LMP, il faut mettre fin au traitement avec RITUXAN. »
AFSSAPS : alertes 2008 et 2010, avec 126 cas de LEMP au total (début 2010 et seulement dans les indications oncologiques)
L’AFSSAPS (l’agence française du médicament, en charge de la pharmacovigilance) a rendue publique le 14 novembre 2008 une mise en garde de la firme Roche quant à un cas de leucoencéphalopathie multifocale progressive à issue fatale survenue sous MabThera° (rituximab). Ce décès « a été rapporté chez une patiente atteinte de polyarthrite rhumatoïde, dans le cadre d’une étude clinique d’extension de tolérance à long terme. »
Cette mise en garde a été reprise dans une lettre aux professionnels de santé, parue sur le site de l’agence, qui informe sur le risque de leucoencéphalopathie multifocale progressive en dehors des traitements pour des lymphomes ou leucémies, et notamment chez des patients traités pour des maladies auto-immunes.
Le point d’information donne des précisions sur le nombre de cas : « Au 29 juillet 2008, 76 cas de LEMP suspectée ou confirmée ont été enregistrés, dans la base de données globale de pharmacovigilance, chez des patients traités par MabThera® dans des indications validées ou non par l’AMM (69 cas dans des indications d’oncologie, 1 cas dans une indication hématologique (anémie hémolytique auto-immune), 5 cas dans les maladies auto-immunes et 1 cas dans une indication inconnue). »
Le 21 janvier 2010, l’AFSSAPS publie d’autres informations sur la sécurité du MabThéra, à partir d’un nouveau décès, et actualise le nombre de cas de LEMP sous MabThéra prescrit dans des cancers.
« Un troisième cas de LEMP a été rapporté chez une patiente atteinte de PR [polyarthrite rhumatoïde], traitée par MabThera®. Contrairement aux cas précédents, ce dernier cas de LEMP a été notifié chez une patiente qui n’avait pas reçu de traitement antérieur par méthotrexate ou par anti-TNF.
L’Afssaps rappelle que MabThera® n’est pas indiqué en première ligne dans le traitement de la PR. »
Nombre total de cas :
« Cas de LEMP sous MabThera® dans des indications autres que la PR : Selon les dernières données disponibles, 126 cas de LEMP suspectée ou confirmée ont été rapportés dans le monde, chez des patients traités par MabThera® dans des indications d’oncologie. Parmi ces cas, sept étaient rapportés en France et vingt six étaient peu documentés. MabThera® était prescrit dans les indications suivantes : lymphome (87), leucémie chronique (28), syndromes lymphoprolifératifs (3) ou maladie de Waldenström (8). Ces patients avaient, en plus de la pathologie sous jacente, le plus souvent des facteurs de risque, tels qu’une prise antérieure de cytotoxiques, d’immunosuppresseurs ou une greffe de moelle.
Par ailleurs, 4 cas de LEMP ont été rapportés chez des patients traités pour une pathologie auto-immune autre que la PR : lupus érythémateux disséminé (2), vascularite (1) et dermatomyosite (1). Quatre cas supplémentaires ont été rapportés dans une indication hématologique (anémie hémolytique auto-immune, purpura thrombopénique idiopathique). (…) »
Quelques autres effets indésirables graves, voire mortels du MabThéra / Rituxan, signalés par Santé Canada
Mai 2001 : annonce de réactions cutanées sévères, dont 8 cas mortels
« II y a eu 20 cas de réactions cutanéo-muqueuses graves liées à I’emploi de ‘Rituxan’ signalés à I’échelle mondiale après la commercialisation. Huit de ces cas ont eu une issue fatale. Ces réactions ont été décrites de façon variable comme un syndrome de Stevens-Johnson, une érythrodermie bulleuse avec épidermolyse, un pemphigus paranéoplasique, une dermatite lichénoïde ou une dermatite vésicobulleuse. La survenue de la réaction dans les cas signalés variait de quelques jours à plusieurs mois après l’exposition à ‘Rituxan’. »
Juillet 2004 : annonce d’une possible réactivation d’une hépatite B, dont certains cas mortels
A noter la nécessité de dépister une hépatite B avant le traitement par rituximab (MabThéra/Rituxan) et d’un contrôle jusqu’à un an après l’arrêt de cet anticorps monoclonal :
« Une réactivation du virus de l’hépatite B (VHB), qui a parfois entraîné une hépatite fulminante, une insuffisance hépatique et la mort, a été signalée chez certains sujets atteints d’un cancer hématologique et traités par RITUXAN, principalement en association avec une chimiothérapie.
Les sujets à haut risque d’infection par le VHB doivent être dépistés avant l’instauration du traitement par RITUXAN.
Les signes cliniques et les résultats de laboratoire indiquant la présence d’une infection évolutive par le VHB et les signes d’hépatite doivent être étroitement surveillés, jusqu’à un an après le traitement par RITUXAN, chez les porteurs du virus de l’hépatite B et les patients qui ont contracté une infection par le VHB mais qui présentent des signes de rétablissement. »
Novembre 2006 : annonce d’occlusions ou perforations intestinales, avec des cas mortels
« Des occlusions intestinales (blocage du petit ou du gros intestin) et des perforations intestinales (apparition d’une ouverture dans le petit ou le gros intestin) ont été rapportées chez des patients traités par RITUXAN®. Certains patients (tous atteints de lymphome non hodgkinien) en sont décédés. Aucune relation entre RITUXAN® et ces événements n’a été prouvée.
Les perforations intestinales sont survenues en moyenne 6 jours après le début du traitement de RITUXAN®. Les patients qui ressentent une douleur abdominale, surtout au début du traitement, devraient communiquer avec leur médecin sans tarder. »
Août 2007 : annonce de deux décès par leucoencéphalopathie (LEMP) chez des patients traités hors AMM pour lupus et un autre cas de LEMP hors AMM pour vasculite
On notera que la firme Hoffmann Laroche met toujours l’accent sur les autres traitements, alors que le lien entre les anticorps monoclonaux et la LEMP est difficilement contestable, d’une part parce qu’il s’agit d’un effet indésirable commun à toute la classe, d’autre part parce que la leucoencéphalopathie multifocale progressive arrive de la même façon chez des patients traités par Tysabri, Avastin, Humira, Enbrel, Herceptin, Raptiva (retiré du marché aussi à cause de cet effet indésirable), Remicade, Cimzia, etc. pour des maladies auto-immunes, et qui n’ont donc aucune chimiothérapie et aucun autre traitement immunosuppresseur…
« Deux (2) décès attribuables à la LEMP ont été signalés chez des patients atteints de lupus érythémateux disséminé ayant reçu RITUXAN [MabThéra]. Les deux patients décédés étaient atteints depuis longtemps de lupus érythémateux disséminé et avaient reçu plusieurs traitements qui empêchent le système immunitaire (le système de défense de l’organisme contre la maladie) de fonctionner avant de recevoir RITUXAN. On a également signalé un (1) cas de LEMP chez un patient atteint de vasculite (inflammation des vaisseaux sanguins) et ayant reçu RITUXAN. Ce patient avait reçu plusieurs traitements qui suppriment le système immunitaire avant et pendant le traitement par RITUXAN. Tous les cas sont survenus dans les 12 mois après la dernière perfusion de RITUXAN. »
Le virus John Cunningham : infection opportuniste cause de la LEMP
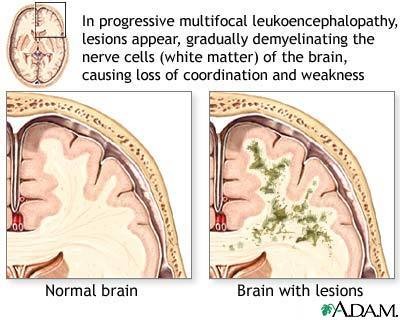
L’illustration accompagne un article du site Pub Med Health sur la LEMP (PML en anglais: progressive multifocal encephalopathy).
Le virus John Cunningham (virus JC) – nommé d’après le patient chez lequel on a isolé pour la première fois ce virus sous sa forme pathogène – est l’agent pathogène responsable de la LEMP, dans les conditions particulières déjà évoquées. L’on estime que 60% à 80% des adultes sont porteurs sains du virus JC, après une première infection pendant l’enfance, habituellement asymptomatique. La période de latence peut être très longue, on parle aussi d’ « infection lente ».
Ce virus JC ne pose aucun problème tant que le système immunitaire fonctionne correctement. Mais il devient pathogène – comme d’autres virus et agents dits « opportunistes » – lorsqu’il y a une immunodépression ou immunosuppression, par exemple en cas de HIV et SIDA, en cas de chimiothérapie, etc. Toutes proportions gardées, les cas de LEMP semblent plus fréquents sous anticorps monoclonaux qu’en cas d’immunodépression due au HIV, où le pourcentage avoisine les 5%, en diminution grâce aux trithérapies antivirales.
La fréquence de la leucoencéphalopathie multifocale progressive chez des patients traités par Rituxan/MabThéra pour un lymphome était estimée en 2007 à moins d’un cas sur 10.000 par Hoffmann Laroche, repris par Santé Canada, qui définit cette maladie ainsi :
« La [LEMP] est une maladie démyélinisante progressive et rare du système nerveux central qui entraîne généralement le décès ou une grave incapacité. La LMP est causée par l’activation du virus JC, qui réside sous forme latente chez 40 à 80 % des adultes en bonne santé. Les facteurs entraînant l’activation de l’infection latente ne sont pas bien connus. La LMP a été signalée chez des patients porteurs du VIH, des patients immunodéprimés atteints d’un cancer, des patients ayant subi une greffe et des patients atteints de maladie auto-immune, dont la polyarthrite rhumatoïde. À l’heure actuelle, il n’existe pas de moyen fiable pour prévenir ou guérir la LMP ». Parmi les symptômes figurent :
- perte de mémoire;
- troubles de la pensée, confusion;
- perte de la vue;
- difficulté à marcher ou à parler;
- convulsions;
- perte d’équilibre ou de coordination.
La mise en garde de novembre 2008 de l’AFSSAPS énumère certains symptômes qui doivent alerter : « des troubles de la vision, des troubles moteurs, une atteinte cognitive généralement associée à une maladresse, une cécité, une faiblesse importante telle qu’une hémiparésie et des modifications du comportement. Les signes additionnels sont des déficits sensoriels, des vertiges et des crises convulsives ».
LEMP et autres effets indésirables graves détaillés sur Pharmacritique
J’ai parlé plus en détail de la leucoencéphalopathie multifocale progressive, et notamment de ses symptômes et de son pronostic, dans d’autres notes sur les divers anticorps monoclonaux, qui rappellent aussi d’autres effets indésirables de toute cette classe (risque augmenté de cancers et troubles lymphoprolifératifs, infections opportunistes, etc.). Ces notes sont accessibles en descendant sur cette page.
Cette maladie est abordée en particulier dans cet article sur les LEMP apparues sous natalizumab (Tysabri°), anticorps monoclonal prescrit dans la sclérose en plaques: « Tysabri: cinq cas de leucoencéphalopathie (LEMP), selon Santé Canada. Rappel du verdict d’Arznei-Telegramm et de Prescrire« .
Critiques fortes par les revues indépendantes Arznei-Telegramm, Prescrire et Butlleti Groc
Dans l’article sur le retrait du Raptiva, j’ai donné deux liens vers des analyses globales des effets indésirables de classe
- une analyse d’ensemble des anticorps monoclonaux, dans l’arthrite rhumatoïde et le psoriasis, a été réalisée déjà en 2005 par la Fundacion del Instituto Catalan de Farmacologia (FICF, auprès de l’Université autonome de Barcelone), qui promeut un usage rationnel des médicaments et effectue des analyses du rapport bénéfices/risques. L’article fort explicite s’appelle « Tocixidad de los farmacos biologicos en la artritis reumatoide y la psoriasis » (Toxicité des médicaments biologiques [issus de la biotechnologie] utilisés en arthrite rhumatoïde et psoriasis). Il a été publié dans le bulletin pharmacologique de la Fondation, Butlleti Groc, membre de l’ISDB (International Society of Drug Bulletins). Il y est question de réactions d’hypersensibilité, d’infections graves, tuberculose et autres infections opportunistes, insuffisance cardiaque, hépatotoxicité, risque de lymphome, troubles neurologiques et hématologiques, risque de réactions auto-immunes, formation d’anticorps contre certains anticorps monoclonaux et d’autres effets indésirables.
- une analyse de moindre envergure et plus limitée, parue en 2004 dans la Revue Médicale Suisse sous le titre « Effets secondaires des traitements par anticorps monoclonaux en hématologie ».
Dans un article sur les leucoencéphalopathies sous Tysabri, j’ai donné les références du verdict de l’excellente revue allemande indépendante Arznei-Telegramm et celui de la revue Prescrire. Je rappelle les conclusions quant au Tysabri (natalizumab):
La revue Arznei-Telegramm a littéralement démoli le Tysabri en août 2006, dès sa réintroduction, dans une longue analyse qui finit par cette phrase: « Puisqu’il n’y a pas de preuves d’efficacité et que l’étendue des risques mortels n’est même pas prévisible, nous considérons que l’utilisation de cette substance toxique devrait être interdite dans une application hors essais cliniques contrôlés randomisés. Pour des raisons éthiques, seule une telle utilisation peut être justifiée, afin de clarifier la question de l’efficacité et de la sécurité d’emploi de la monothérapie par cet anticorps chez les patients correspondant aux indications » (a-t 2006; 37: 69-71, réservé aux abonnés).
Ce n’est pas tout.
Un article de février 2007 (a-t 2007; 38: 17) donne le Tysabri et quelques autres comme exemples d’autorisation hâtive et sans vérification du rapport bénéfice – risques, preuve de la servilité des agences du médicament envers les firmes dont elles dépendent financièrement. Une brève de février 2008 (a-t 2008; 39: 24) pose la question de deux cas de mélanomes signalés aux Etats-Unis. En juillet 2008, il est question de plusieurs dizaines de cas de troubles hépatiques, de sévérité diverse (a-t 2008; 39: 80).
Enfin, en décembre 2008, Arznei-Telegramm rend compte (a-t 2008; 39: 126) d’un deuxième décès par LEMP, signalé par la firme Genentech (…), qui reconnaît enfin que le médicament pourrait augmenter le risque de leucoencéphalopathie. (Alors qu’on le savait depuis les essais cliniques, vu les décès ayant entraîné le retrait du marché de 2005, mais qui ont fort opportunément disparu de la comptabilité… Est-ce raisonnable de passer l’éponge sur une telle « préhistoire » d’un médicament?)
A quand une évaluation globale par des experts indépendants ?
Je ne peux que reposer la même question : au vu de tous ces cas d’effets indésirables graves et de décès, qu’attendent les autorités sanitaires pour mettre en place une révision globale de l’ensemble de la classe des anticorps monoclonaux, quelle qu’en soit l’indication ?
Parce qu’après les promesses de Xavier Bertrand, et même s’il n’en reste plus grand-chose dans le projet de loi (voir les critiques ici et là) nous sommes en droit d’exiger une évaluation correcte de ces biomédicaments extrêmement chers et faisant l’objet d’un marketing de plus en plus agressif. Une expertise faite sous l’angle du rapport bénéfices/risques, mais aussi sous l’angle du rapport coût/efficacité.
Progrès thérapeutique faible
Je rappelle que lorsque l’un de ces anticorps a fait l’objet d’un avis de la Haute autorité de santé, l’amélioration du service médical rendu (ASMR) a été jugée faible, voire très faible, pour la plupart d’entre eux. Le niveau I (progrès thérapeutique majeur), attribué à l’association MabThéra + chimiothérapie dans le traitement d’un certain type de lymphomes, est exceptionnel.
Mais le rapport bénéfices/risques n’est pas le même dans le traitement d’un cancer et dans le traitement d’une maladie auto-immune (arthrite rhumatoïde, sclérose en plaques, lupus, psoriasis, maladie de Crohn…) Et compte tenu de la promotion agressive par les firmes, on peut s’attendre à ce que tous ou presque obtiennent des extensions d’indication. S’il est raisonnable de prendre certains risques dans un cas de cancer, si le traitement permet des bénéfices importants, cela ne l’est pas dans une maladie chronique. Il est même assez cruel d’exposer les patients à un risque de lymphome en leur administrant un traitement utilisé dans les lymphomes.
Ne faisons pas des malades chroniques des cobayes. Cela dit, je n’ignore pas que des associations de malades ayant des conflits d’intérêts sont instrumentalisées par l’industrie pharmaceutique et par les leaders d’opinion qui composent leurs comités scientifiques et font de la publicité pour des anticorps monoclonaux (aussi dans la variante anti TNF alpha, comme on l’a vu récemment avec l’Association française des polyarthritiques, associée à Abbott, Sanofi-Aventis, Schering-Plough, Roche, BMS… Ou encore lors de la campagne de « sensibilisation » sur les spondylarthropathies, où les militants associatifs se sont associés à la Société Française de Rhumatologie et à Pfizer et ont fait appel à Franck Leboeuf (campagne « Dos au mur »).
Si même la très généreuse Haute Autorité de Santé – qui n’a jamais contesté l’AMM d’un médicament pour une ASRM (amélioration du service médical rendu) nulle, mais a toujours trouvé un moyen de reconnaître un minimum d’intérêt – juge l’apport de ces médicaments peu satisfaisant, on peut s’attendre à ce qu’une évaluation par des experts moins complaisants et indépendants ait des résultats dévastateurs pour le chiffre d’affaires de Roche, Abbott, Sanofi-Aventis et autres Novartis et Pfizer.
**
Mise à jour de 2017
En août 2017, l’ANSM à rendue publique une brochure d’information conçue par le laboratoire pharmaceutique Sandoz, filiale de Novartis. Elle présente les indications du rituximab et les grandes lignes des autres informations obligatoires, puis explique la survenue possible de leucoencéphalopathie multifocale progressive.

Elena Pasca
Copyright Pharmacritique

Le rituximab a changé la donne dans la prise en charge de certains lymphomes en améliorant de façon significative le pronostic des patients.
Dans le lupus, c’est un échec et j’ai tendance à penser qu’il doit être réserver à des cas particuliers en sauvetage. Une indication va émerger, ceux sont les vascularites à ANCA où il fait aussi bien que l’endoxan mais pas mieux en terme de complications. C’est un produit efficace non dénué d’effets secondaires mais qui est utilisé dans des maladies graves voir très graves. Je connais peu de médicaments efficaces qui ne sont pas dénués d’effets secondaires. Je suis un chaud partisan de son évaluation dans des essais de bonne qualité méthodologique d’autant plus que ce monoclonal là va être dans ma spécialité probablement encore plus utilisée.
Il est bien de tirer la sonnette d’alarme sur les effets secondaires des médicaments, mais je pense qu’il faut tenir compte de la balance bénéfice risque.
Je prescrit du rituximab uniquement hors amm, j’informe toujours les patients des risques et des bénéfices attendus en leur expliquant que j’ai peu ou pas d’études mais de bonne raison de penser que ce médicament va être efficace.
Concernant le prix, il s’agit d’une négociation entre le labo et le payeur.
J’aimeJ’aime
Bonjour Stéphane et merci pour ces remarques fort utiles.
Les usages hors AMM
Ils ne me posent pas de problèmes s’ils sont justifiés et ne résultent pas des conflits d’intérêts des médecins prescripteurs et de leurs sociétés savantes ou de leurs établissements et ne sont pas non plus juste une traduction en pratique du marketing des laboratoires.
J’en ai parlé au passage en abordant les recommandations de bonne pratique et mon inquiétude à les voir devenir opposables (c’est le même problème, sous un autre angle). La liberté de prescription me semble essentielle, même si je ne suis qu’une usagère lambda.
De même, voir Xavier Bertrand se focaliser sur les prescriptions hors AMM, à cause du Médiator qui a été prescrit comme coupe-faim, m’inquiète aussi. J’y reviendrai, car c’est l’un des sujets sur la liste, trop longue, de ceux qui seront abordés sur Pharmacritique.
Evaluation globale
Nous sommes d’accord; je n’arrête pas de déplorer l’absence d’une telle évaluation et les AMM trop rapides – des extensions d’indication, très souvent -, sous la pression d’associations instrumentalisées par l’industrie pharmaceutique comme des sociétés savantes ayant des conflits d’intérêts avec celle-ci.
S’il y a de telles évaluations – essais cliniques randomisés, contrôlés, en double aveugle + méta-analyses, plus expertises indépendantes… – et qu’elles montrent une efficacité incontestable, un rapport bénéfices/ risques et coût / efficacité favorables, eh bien, j’en serais ravie pour les patients! En attendant, c’est déjà une question de principe que de questionner les AMM obtenues dans de telles conditions, surtout par extension d’indication qui est un problème en soi, lié aux points déjà abordés, et au rapport bénéfices/risques. Elle se fait beaucoup trop facilement – pas besoin d’être médecin pour le comprendre.
Rapport bénéfices/risques
Nous sommes d’accord, et j’ai d’ailleurs complété le texte en ce sens. Mais en disant quand même que ce rapport peut être favorable s’agissant de prescriptions dans des cancers, où il peut être raisonnable de prendre certains risques et en disant aussi que le rapport bénéfices/risques n’est plus le même dans des maladies telles que le lupus, l’arthrite rhumatoïde, etc. Le niveau très faible d’ASMR (amélioration du service médical rendu) dans ces maladies est une preuve de plus.
Parlant d’évaluation, j’ai ajouté une bonne demi-page pour rappeler celles faites par les revues indépendantes de qualité: Arznei-Telegramm, Prescrire, Butlleti Groc. Toutes les trois sont très critiques à l’égard des anticorps monoclonaux, et elles ne sont pas les seules.
Par ailleurs, Arznei-Telegramm a encore reparlé du Tysabri récemment (à propos d’autres cas de LEMP); ça viendra sur Pharmacritique aussi.
Je crois que nos positions ne sont pas incompatibles sur l’essentiel.
Au plaisir de vous lire
J’aimeJ’aime
Bonjour ELENA
PRESCRIPTIONS HORS AMM
http://www.fdn.fr/~amagnouat/metge/spip.php?article102
TRES IMPORTANT
Informer davantage les patients : mentionner le « hors AMM »
sur l’ordonnance
Cliquer pour accéder à 31_mai_2011_-_Synthese_des_propositions_du_groupe_3.pdf
http://questionsdesante.hautetfort.com/archive/2011/02/24/dossiers-medicaments-prescription-hors-amm-et-responsabilite.html
Tout prescription hors AMM doit s’accompagner d’une information du patient par le médecin : qui sur l’ordonnance se traduira par l’apposition de l’abréviation « NR » (Non remboursable) à côté de la dénomination de la spécialité (Art. L. 162-4 et L. 162-8 du code de la sécurité sociale).
Quoi qu’il en soit il faut toujours lire la notice du médicament vérifier sur internet (prescrire…….)
Donc ne pas faire confiance sans avoir vérifié le bien-fondé de cette prescription
Cordialement
Martine
J’aimeJ’aime
Merci pour ce article, car on peut se poser beaucoup de question concernant le traitement de la polyarthrite rhumatoïde: l’AFPric- dont vous parlez-, association reconnue d’utilité publique, promeut fortement les biothérapies.
Elle suit en cela une partie de la Société Française de Rhumatologie, dont les « leaders d’opinion »-professeurs de médecine,voient leurs recherches pratiquement entièrement subventionnées par l’industrie pharmaceutiques.
De la même façon, je viens de constater en vérifiant les subventions des laboratoires aux associations, désormais publiées sur le site de l’AFSSAPS,et les comptes publiés sur le site de cette asso, que ces dons de l’industrie pharmaceutique équivalent pratiquement aux cotisations des adhérents…dons ou publicités publiées, je suppose, dans la revue de l’association, pour recommander ces biothérapies. Du coup, celle-ci pourrait-elle vivre sans ça, j’en doute.
La boucle est bouclée: sommes nous informés?
Quand un de vos proches est atteint de cette terrible maladie, il est crucial d’avoir une information digne de foi.
Vers qui se retourner, alors, sinon vers les associations de patients?
N’est-ce pas là un conflit d’intérêt inadmissible? si cette association alertait sérieusement sur les effets secondaires multiples et graves, et non anecdotiquement, ce serait de l’information: mais il est évident qu’elle perdrait alors sa place de relais de l’industrie pharmaceutique et ses mannes.
L’afssaps vient d’ailleurs de retirer deux recommandations sur la prise en charge de la maladie, ce qui ajoute à la confusion.
Qui croire?
J’aimeJ’aime
Vous avez de toute évidence passé quelque temps sur ce sujet. Bien vu! Ceci est un poste de grand!
J’aimeJ’aime
C’est pas rassurant comme information, mon père en en train de prendre un traitement de MabThéra. Encore il n’est pas pris en charge, je peux vou le garantir que c’est cher. Et la première perfusion lui a fait un effet sur son coeur, mais après c’est passé.
J’aimeJ’aime
Bonjour,
J’ai 30 ans et je suis moi-même traitée sous MabThéra pour une PR sévère.
Il est certain que parmi les rhumato, tous s’accordent sur la Révolution que représentent les biothérapies.
Votre article est inquiétant et peut semer la panique parmi les patients traités avec cette bio.
Cependant, je pense qu’il est nécessaire de prendre du recul.
Comme il a été dit plus haut, quel médicament efficace n’entraîne pas potentiellement des effets secondaires ?
Les rapports médecins / associations de patients / industries pharma tels que vous les décrivez ne paraissent pas dénués de sens… Mais tout de même ! Pardonnez ma naïveté, j’ai peine à croire que mon rhumato me prescrirait du MabThéra (PR sur patient jeune !) pour un histoire de gros sous ?!!
[NdR: PR = polyarthrite rhumatoïde]
J’aimeJ’aime
je suis myasthenique. on me preconise ce traitement pour la rentree a lors actuelle je suis traitee avec de la tegeline toute les quatre semaine.
je ne sais quoi penser.
merci de m eclairer.
merci
[NdR: nom de famille effacé par prudence, s’agissant de données médicales personnelles. Un prénom (ou pseudonyme) suffit sur internet]
J’aimeJ’aime
Atteint d’un lymphome de bas grade (B) depuis 4 ans, je n’ai jamais été traité….., je vais faire ma première injection dans qq jours, suivie de 3 autres à 1 semaines d’intervalle. Advienne ce que pourra!.
J’aimeJ’aime
Bonjour
Merci pour cette longue information.
J’aurais bien aimé la trouver avant mon lymphome en février 2010.
Heureusement je n’ai eu qu’une chimio (CHO-Mabthéra), sur huit programmées, car j’ai refusé les suivantes.
Patrick
J’aimeJ’aime
Bonjour,
J ai pris du mabthera en 2005 pour une forme sévère de lupus avec atteinte rénale. Dans l année qui a suivi j ai commencé à avoir des infections à repitition dont 3 pneumonies. Puis le diagnostic est tombé hyppogammaglobulinemie liée vraisemblablement au mabthera. Cela fait maintenant 7 ans que je dois traiter cette maladie supplémentaire. Je pense qu il est essentiel d informer les patients et de ne pas prescrire un médicament sans connaître les bénéfices réels sur une maladie.
J’aimeJ’aime
bonjour,
Je me souffre d’une polyarthrite sévère, connue depuis 1998. J’ai eu en traitement mise à part la cortisone, arava, novatrex (arrêt pour hépatite médicamenteuse), plaquenil (arrêt pour urticaire géant) ensuite rémicade, arrêté pour opération d’un cancer du sein en avril 2011, cancer du poumon décelé en décembre 2011 , opéré en février 2012.
On me propose pour février 2013 mabThéra. Je viens de lire l’article sur ce médicament et j’avoue que l’ai un peu peur quand même du résultat. Que dois-je faire accepter ou non???? Pourriez-vous m’en dire davantage et me donner votre avis après tous les traitements que j’ai eu et les cancers opérés.
Merci par avance.
J’aimeJ’aime
Bonjour,
J’ai été traité au Rituximab pour un purpura thrombopénie idiopathique, soit une maladie bénigne. Avec le recul, et d’autant plus après la lecture de cet article je regrette de m’être laissé influencé par mon hématologue qui m’a indégniablement mis une certaine pression pour que j’accepte le traitement. Et qui de surcroît, l’a fait passer pour une ultime alternative à l’ablation de la rate alors qu’en réalité le traitement ne fait que reculer cet acte de 2 ou 3 ans. Les effets secondaires que j’ai vécu à court terme et les doutes qui planent toujours sur ses potentiels effets secondaires à moyen et long terme et me font clairement dire dans le cadre d’un PTI le rituximab est un mauvais choix.
J’aimeJ’aime
Mon papa est décédé ce 31 décembre des suites d’une hépatite fulminante. Une autopsie est en cours. Il avait été traité par chimiothérapie et anticorps monoclonaux suite à un lymphome non-hodgkinien à grandes cellules. Son traitement était terminé depuis fin avril et il l’avait toujours bien supporté. L’oncologue l’avait déclaré en rémission et voilà qu’une hépatite B aigue se déclare en novembre. Fin décembre, mon papa nous quittait sans avoir jamais eu de transfusion sanguine qui expliquerait la contamination. L’intoxication au paracétamol, aux champignons et à l’alcool ont également déjà été exclue. Je me demande donc dans quelle mesure le traitement par anticorps monoclonaux n’est pas en cause dans son décès. Je vous tiendrait au courant dès que les résultats de l’autopsie me seront parvenus (dans deux mois).
J’aimeJ’aime
helas , ces anticorps monoclonaux peuvent parfois induirent des pathologies serieuses, mais ce n’est pas le cas pour tous et la grande majorité d entre nous ont un benefice serieux……il faut en effet mesurer le risque de prendre ces specialitées et la possibilité de s’en passer , est ce que votre pronostic vital est engagé, est ce que votre maladie auto immune est trop invalidante pour vivre sans ce traitement…..
je vous dirai juste une chose ,il y a des persones qui ont des patho auto immmunes non connus par la medecine , c’est mon cas , ou des maladies rares ……nous n’avons rien pour etre soulager ,et attendons beaucoup de ces specialitées,car la vie est impossible, beaucoup d’entre nous rennoncent a la vie car la torture est permanente ….
nous avons l encephalomyelite myalgique , appelé communemment « syndrome de fatigue chronique » la norvege a decouvert son origine auto immune en 2009 !! depuis deux siecles de medecine les gens etaient orientés en psychiatrie !! imaginez vous souffrez d’une vraie maladie et tout les medecins vous rient au nez en disans c’est dans votre tete, allez bougez faites du sport ça va aller mieux !!! voila , donc si j’avais eu le choix , j’aurais bien aimer avoir une maladie moins invalidante et connu par la medecine
J’aimeJ’aime
Bonjour,
on m’a diagnostiquée un lymphome folliculaire de bas grade stade 3 en juillet 2011 et j’ai terminé il y a peu mes cures de chimio CHOP-MABTHERA. Je suis désormais à ma 4ème injection de MABTHERA d’entretien seul.
Malheureusement je ne me pose que trop tard la question du bénéfice/risque de ce traitement, et sûrement que j’aurais dû m’interroger davantage à son sujet. J’ai fait une réaction allergique lors de la première perfusion en association avec CHOP, mais que l’on pourrait dire « classique ». Par contre il n’en est pas de même depuis que je fais le traitement d’entretien seul. Au fur et à mesure des perfusions mes troubles s’intensifient, mais il m’a fallu longtemps pour faire le lien, et poussée par les médecins j’ai oublié de m’écouter. Je souffre désormais de troubles hépatiques, douleurs abdo et à l’estomac, nausées, vomissements, vertiges, rougeurs, diarrhées, ballonements. Les douleurs sont parfois insupportables et mettent beaucoup plus de temps à disparaître qu’à apparaître.
Je suis également infirmière, et connaiS donc les deux côtés de la barrière, d’autant plus que j’ai travaillé en hémato/oncologie. Effectivement, on ne peut pas nier qu’il y a des histoires de gros sous avec les labos, les médecins, les intervenants de pharmacovigilance. Depuis que j’ai ces soucis, quelles difficultés j’ai à me faire entendre!!! C’est une bataille de chaque jour, ou malgré le fait que j’ai énoncé clairement vouloir arrêter le traitement, on me répond qu’on ne va le faire que temporairement.
Effectivement, mes premières questions sont : sommes nous des cobayes à notre insu? Concernant ce traitement et à la vue de mon parcours de soins, réellement je pense que des choses qui nous échappent totalement en tant que patient se jouent. Lors des derniers symptômes j’ai cru que j’allais y rester, j’ai toujours le sentiment que si je refais une perfusion je vais y laisser ma peau. C quelque chose de très fort.
Si je n’ai qu’un conseil à donner dans ce que vous vivez et dans cette décision de faire ou non du Mabthera, c’est d’écouter ce que vous dit votre corps et non votre tête, il est le meilleur indicateur possible et le plus fiable. Faites confiance à votre ressenti trop souvent oublié, il ne peut que vous aider et vous évitera de perdre votre temps. Il vous évitera surtout parfois de vous laisser mener et de faire le mouton, ou de suivre des moutons car en tant que soignants (médecins, infirmières, aide-soignants…) nous sommes préformatés par nos écoles à être des moutons.
J’aimeJ’aime
bonjour,
j’ai 54 ans, et un syndrome de Sharp depuis 30 ans, traité par plaquenil avec des manifestations articulaires et un syndrome de Raynaud. Sont venues s’ajouter dans le temps une hypothyroïdie d’Hashimoto ainsi qu’une surdité d’origine auto-immune, un syndrome de Gougerot-Sjögren, et il y a deux ans une polymyosite dite de recouvrement.
Pour la PM, j’ai été traitée par bolus de corticoïde associé à 40 mg de cortancyl et 20 mg de méthoject étalés sur un an et demi, jusqu’à l’arrêt du traitement et la reprise du plaquenil. Quelques mois plus tard : rechute et donc à nouveau bolus + méthotrexate + 5mg de prednisone. Aujourd’hui, deux mois se sont écoulés, les cpk sont de nouveau à 3000 et les transaminases sont élevées.
Le médecin envisage de passer au Mabthéra. Que dois-je faire ? Merci de me donner votre avis. Cordialement.
M.Françoise
J’aimeJ’aime
Bonjour Françoise,
malheureusement PHARMACRITIQUE n’est pas un site de consultation hyper spécialisé, et vos soucis de santé relèvent d’avis pluridisciplinaires…
Tous les traitements déjà pris sont déjà lourds et bourrés d’effets secondaires.
Ces anti-corps chimériques n’ont pas fait jusqu’à maintenant la moindre preuve d’une balance bénéfice-risque favorable, et les gains faibles que vous pouvez en attendre seront contrebalancés pas des effets secondaires auxquels vous n’échapperez pas.
Mais mon confrère est au désespoir et ne sait plus quoi faire, alors on y va!
Sachez que ce traitement dans votre cas relève plus de l’expérimentation et discutez-en sérieusement avec votre médecin. Si vous les prenez tenez-nous informer, d’autres patients étant intéressés.
Cordialement et vous souhaitant une amélioration.
PS : relisez les articles de Elena PASCA qui a créé ce blog. Et existe-t-il une association syndrome de Sharp qui ait des information?
J’aimeJ’aime
Mon mari a été traité pendant 7 ans pour un lymphome folliculaire stade IV, il a recu plusieurs cures de mabthera.
Il est aujourd’hui atteint d’une LEMP. Son bras gauche a commencé à s’engourdir il y a trois mois, et à ce jour il est totalement hémiplégique.
Si son oncologue avait vaguement souligné le caractère quelque peu expérimental de son traitement, il n’a jamais evoqué les possibles effets secondaires très grave de ce produit. Même alors que le diagnostique de lemp est établi avec certitude depuis une dizaine de jour et que le neurologue nous a conseillé de règler nos affaires personnelles au plus vite, personne ne semble mettre en cause directement le mabthera. Chacun se contente de nous expliquer que la lemp peut se développer chez les patients immunodéprimés. Or il m’a suffit de quelques clics pour découvrir les liens entre cette horreur qu’est la lemp et le mabthera. Le laboratoire roche lui même admet qu’environ 130 personnes traitées par mabthera ont développé une lemp. Certes ce n’est pas énorme au regard des bénéfices que ce produit a peut etre apporté à certains, mais je me demande pourquoi personne ne nous a jamais parlé de ce risque. Chez les malades souffrant de SEP [NdR: sclérose en plaques] la recherche du jc virus (responsable de la lemp) se fait automatiquement car on sait que certains traitements pour la SEP comporte un risque de développement de lemp. Mon mari ayant déjà fait ce qu’on croyait être un avc ( mais qui selon le neurologue aujourd’hui était dejà le début de la lemp) il y a trois ans, pourquoi personne ne nous a alerté et proposé autre chose que du mabthera???
Je sais bien qu’incriminer les médecins n’empechera pas mon mari de mourir et qu’il serait peut être déjà mort s’il n’avait pas eu ce traitement, mais j estime qu’on aurait du nous informer, nous laisser choisir en toutes connaissance de cause.
J’aimeJ’aime
bonjour.
en regard de la liste de tous ces commentaires sur le Mabthera, on peut effectivement prendre peur et avoir peur!
Actuellement traité (5ème chimio faite ce jour, sur 6 initialement programmée) avec du mabthéra , associé à de l’endoxan + fludarabine pour une Maladie de Waldenstrom, je ne sais que penser , d’autant plus qu’un grand spécialiste de cette maladie , exercant sur Paris ,à juge que le traitement que je recevais (ville de province) était un bon traitement.
Alors qui croire et que faire, sinon faire confiance ? à qui s’adresser pour etre sur ?
beaucoup de questions et interrogations nous interpellent en lisant tout ces différents commentaires!
10.07.2014
J’aimeJ’aime
J’ai une polimyosite musculaire sa fait 1 ans . Je suis sous corticoïdes cortancyle 12,5 mg, j’avais un traitement imurel qui me fessais plus effet. Je passe a methotrexat a 15mg . Deux mois de traitement ne me font plus d’effet ils veulent que je fasse le traitement du mabthera . si quelqu’un pouvait me dire quelque chose sur ce traitement dont j’ai peur uc les commentaires
J’aimeJ’aime
Suite à un traitement rituximab, je me suis retrouvé en réa pour décompensation cardiaque, le traitement à été repris par chop et rebelote réa et à ce jour je me retrouve avec une insuffisance respiratoire, sous oxygène 24h/24, avec très peu de résultat pour la maladie de waldenstrom, que pensez alors que tous les médecins font le dos rond et ne répondent absolument pas à toutes mes questions, à savoir est ce que cet état va être reversible?
J’aimeJ’aime
Bonjour moi même je suis une personne traitée pour une pr avec mabthera et je trous de mémoires, j’oublie ou je vais je suis pas concentrée c’est comme il mon effacer le mémoire même pas si j’ai passer cette rue ou pas ma gorge est serré j’arrive pas à avaler des fois changement de vois qui disparue quant il fait chaud des migraines insupportables, quant je fais ce médicament mon bras gauche me fais mal avec des fourmies dans mes doigts j’ai fais une allergie une fois. Et j’ai signaler ça à mon médecin ils ma fait une irm et il m’a dit c’est pas inquiétant mais moi toujours je me plein de trouble de mémoires car j’avais pas ça avant donc qu’est que je dois faire??? Merci de me répondre
J’aimeJ’aime
bonjour,
merci pour ces infos. Vous évoquez le Remicade parmi les traitements de biothérapie.
Cela fait 2 ans que je suis sous ce traitement pour une SP [NdR: spondylarthrite] ankylosante.
Dois-je m’inquiéter pour la suite…
Merci de votre réponse
Cordialement,
Mme B.
[NdR: Nom de famille effacé par Pharmacritique, par prudence, s’agissant de données personnelles. Un prénom suffit sur internet].
J’aimeJ’aime
Bonjour,
Bonjour,
je suis sous le biologique rytuxan, j’ai une grosse perte de poids en gras et je suis tres inquiete. Je ne sais pas quoi faire. Y a-t-il quelqu’un dans la même situation? Y a-t-il une personne qui peut me conseiller?
Merci .
[NdR: Nom de famille effacé par Pharmacritique, par prudence, s’agissant de données médicales. Un prénom suffit sur internet]
J’aimeJ’aime
Mon papa, souffrant d’un SAPL de type lupique avec depuis un an une thrombopénie sévère (purpura thrombopénique immunologique ) s’est vu proposé un protocole de 2 perfusions de Rituximab à 15 jours d’intervalle accompagnés au préalable par une série de vaccins; qu’il accepté. A part les effets secondaires, il n’a été a aucun moment préisé les risques de mortalité.
Tandis qu’il souffrait d’insuffisance rénale chronique, et de soucis cardiaque de longue date, nous avions également des signes d’atteintes sur la mémoire et le moral.
Il était dans un état émotionnel diminué, souffrant notamment de nombreux doutes sur les traitements qui lui ont été administrés durant cette dernière année où la maladie prenait de l’ampleur (corticothérapie, plaquenil…). En mars, il se remettait difficilement d’un œdème pulmonaire et supportait assez mal les derniers traitements (cortisone, lasilix, essoufflement, fatigue, tristesse…).
Lors de son dernier RDV de suivi début avril, suite aux 2 transfusions, il lui a été simplement dit qu’il n’y avait plus qu’à attendre; de voir si le traitement rituximab agissait ou pas.
Attendre.
3 semaines après. après 2 nuits et journées de souffrance, mon papa est décédé d’insuffisance cardiaque ce dimanche 29 avril après midi aux soins intensifs de cardiologie d’Avignon. Nous n’avons rien pu faire. Aucune explication n’est donnée, sauf qu’il était « fatigué ».
Je ne peux que faire le lien avec le Rituximab, traitement lourd de conséquence, qui a finit de le vider de son énergie. Pour les médecins et spécialistes qui le suivaient, il n’y a aucune relation à faire. Pour ma part, je pense que cette prescription n’a pas été anodine, dans son cas précis.
J’aimeJ’aime
Notre fille a arrêté le Rituximab il y a 3 ans pour une maladie auto immune qui a attaqué ses reins. Depuis elle ne fabrique plus d’Immunoglobulines. Avez-vous trouvé une solution pour refaire marcher correctement votre système immunitaire depuis votre post ?
J’aimeJ’aime
Ma mère souffre d’une purpura thrombopénique immunologique depuis 6 mois avec traitement en corticoide sans resultat.
Son medcin a proposé MabThéra, le lundi dérnièr (24/09/18) a fait sa 1ère secance. Elle sent très épuisé, fatiguée…malheuresement, aujourd’hui le jeudi a commancé à sentir mal au dos et des difficultés respiratoires.
Je pose la question s’elle doit continuer les 3 seances restantes ou non! avec tout les commentaires que j’ai lu, je suis vraiment choqué.
J’aimeJ’aime